では、第4はあるのでしょうか?言い換えるなら、医学は全ての前癌性ポリープを同定したのでしょうか?
そもそも、未知のポリープを予測することは可能でしょうか?・・・・・全ゲノム解読が、これを可能にします
遺伝子解析で大腸癌の全貌が解明されて・・・・
私が分子生物学の研究をしていた30年前は「癌で変異している遺伝子はあまりにも多く、全貌解明は不可能」と考えられていました。しかし300人の大腸癌の全ゲノムを解読した結果(米国TCGAプロジェクト 下図)現在は「癌化のメカニズムは、実は驚くほど単純だった」と多くの研究者は考えています。
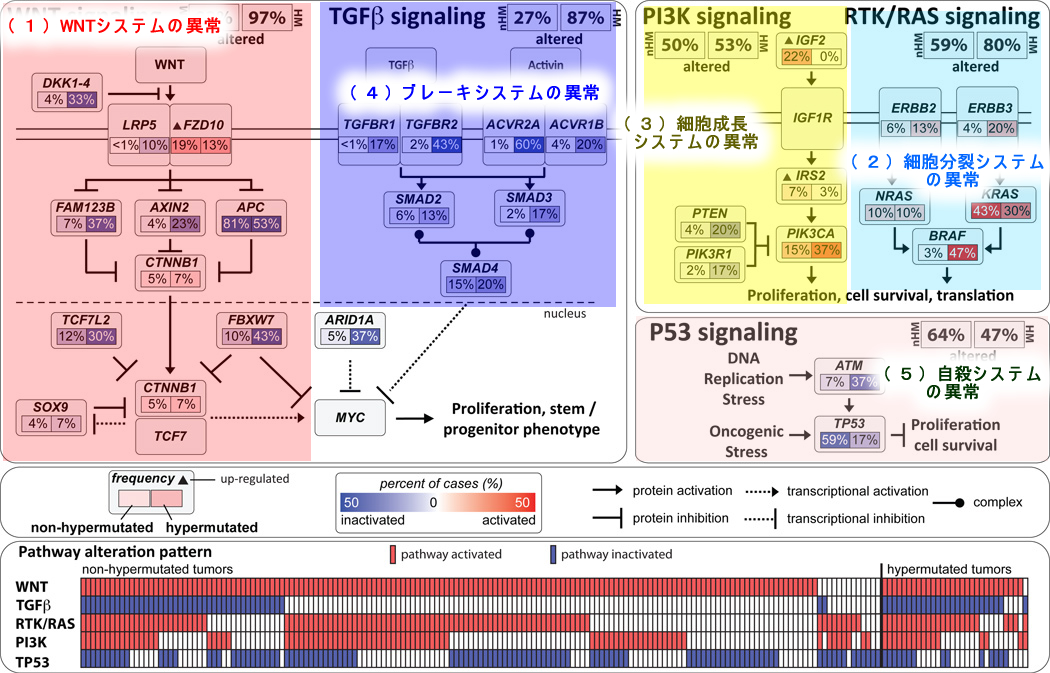
大腸癌の全遺伝子解読から、ほぼ全ての大腸癌は、以下の「5つのシステム異常」により発生することが解ったのです
(1)WNTシステムの異常(幹細胞化)
(2)細胞分裂システムの異常(RAS/RAF/MAP伝達系の亢進)
(3)細胞成長システムの異常(PI3K/TOR系の亢進)
(4)ブレーキシステムの異常(TGFβ系の破壊)
(5)自殺システムの異常(p53系の破壊)
人の癌で見つかる主要な遺伝子は300種類あり(癌化の原因になりうるのは約3000と予想)多岐に渡ります。しかし、どの遺伝子であれ、大腸癌では結局は、この、どれかのシステムの異常に帰結されます。「個々の遺伝子の異常」ではなくて、「システムの異常」が癌化の本質だった訳です(The Cell 6版より)
抗癌剤耐性になったり、幹細胞化して転移するには、更に別なシステム異常(エピゲノム異常)が必要なのですが、「大腸癌発生」はこの「5つのシステム」が主要ドライバーです。因みに他の多くの癌では、「Rbシステムの異常が一般的」で、「WNTシステムの異常」は見られません。大腸癌とは「WNTシステムが異常になり、Rbシステムが正常な癌である」とも言えます。また、胃癌も「WNTシステム異常」であることが報告されました。胃癌も「大腸癌と同じタイプ」と言えます


