傑偢俀侽俀侾擭偵嫽枴怺偄曬崘偑Cell偵偁傝傑偟偨丅杮僒僀僩偱傕丄壗搙傕庢傝忋偘偰偄傑偡偑乽態庮偺娻壔乿偲乽夁宍惉億儕乕僾乮SSAP)偺娻壔乿偺懳斾偱偡丅
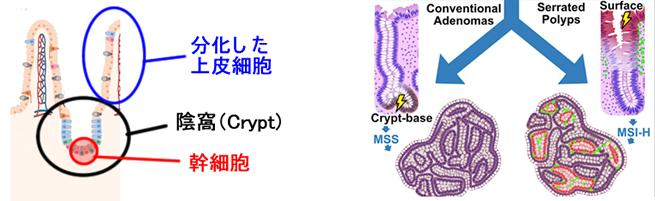
撪梕偼丄崱傑偱偺曬崘偺廤戝惉偲偄偆傋偒傕偺偱偡丅乮佀SSAP偺堓忋旂壔惗丄佀態庮偼戀帣壔丄SSAP偼榁壔偱偁傞乯
態庮偼乽堿鈢偺嵟怺晹乿偱乽姴嵶朎偺庮釃壔乿偱惗傑傟傑偡丅
懳偟偰乽夁宍惉億儕乕僾乿偼乽堿鈢偺昞憌晹乿偱乽暘壔偟偨忋旂嵶朎乿偑丄孞傝曉偡墛徢巋寖乮挵撪嵶嬠偑廳梫側尨場乯偱乽堓忋旂壔惗乿傪婲偙偡偙偲偱惗傑傟傑偡丅SSAP傗TSA乮嫎帟忬態庮乯偺弶婜偼夁宍惉億儕乕僾偱偡偐傜丄弌帺偼摨偠偱偡丅
偮傑傝丄戝挵偺庮釃偺弌帺偵偼乽姴嵶朎儖乕僩乿偲乽堓忋旂壔惗儖乕僩乿偺擇偮偑偁傞丄偲偄偆堄尒偱偡丅
師偵俀侽俀俀擭偵擔杮偐傜嫽枴怺偄曬崘偑Nature偵偁傝傑偟偨丅
孞傝曉偡墛徢巋寖偼乽姴嵶朎偺屚妷乿傪堷偒婲偙偟傑偡丅偡傞偲姴嵶朎偵椬愙偡傞乽慜嬱嵶朎乮Committed乯亖彮偟偩偗暘壔偟偨丄偲偄偆堄枴乿偑儕儕乕僼偲偟偰姴嵶朎偵曄傢傝傑偡丅偙傟偑丄岆偭偨暘壔傪偟偰乽壔惗偺尨場偲側傞乿偲偄偆曬崘偱偡丅曬崘偱偼乽p57(+)嵶朎乿偲偄偆堿鈢偺怺晹偵偁傞慜嬱嵶朎偱挷傋偰偄傑偡偑丄懠偺偁傜備傞慜嬱嵶朎偑丄姴嵶朎儕儕乕僼偲側傝壔惗偺尨場偵側傞偺偩傠偆弎傋偰偄傑偡丅
| 乽姴嵶朎屚妷乿佀乽姴嵶朎儕儕乕僼乿佀乽庒曉傝乮Reprogramming乯乿佀乽壔惗乿佀乽敪娻乿 |
| Cell偺曬崘偱偼乽堓忋旂壔惗偼堿鈢偺昞憌偱婲偙傞乮Surface敪娻乯乿丄Nature偺曬崘偱偼乽堓忋旂壔惗偼堿鈢偺怺晹偱婲偙傞乮Bottom敪娻乯乿偲偄偆揰偑媡偱丄崱屻丄榑憟偵側傞偲巚傢傟傑偡丅 幚偼摨偠榑憟偑堓偺挵忋旂壔惗偱悢擭慜偐傜懕偄偰偄傑偟偨丅 堓偺挵忋旂壔惗偺婲尮偼乽堓偺庡嵶朎乮暘壔偟偨嵶朎乯偺庒曉傝乿偲偄偆偺偑掕愢偱偟偨偑丄搶戝偺僌儖乕僾偑乽庡嵶朎偱偼側偔偰慜嬱嵶朎偺姴嵶朎傊偺庒曉傝偑婲尮乿偲曬崘偟偨偺偱偡乮2020擭曬崘乯丅偦偺屻2021擭偵偼乽傗偼傝庡嵶朎偑挵忋旂壔惗偺婲尮乿偲偄偆斀榑偑弌偰丄2022擭Review偼廬棃偺乽庡嵶朎愢乿傪嵦梡偟偰偄傑偡丅寛拝偼夝傝傑偣傫偑擔杮偺尋媶幰偑悽奅傪憡庤偵榑憟傪婲偙偡偙偲偼慺惏傜偟偄偙偲偱偡丅 偄偢傟偺応崌偱傕丄暘壔偟偨嵶朎偑丄嵞傃枹暘壔側忬懺偵擖傝乮庒曉傝乯丄嵶朎暘楐偵擖傞尰徾偼Paligenosis 偲屇偽傟傑偡丅僆乕僩僼傽僕乕偵傛傝暘壔嵶朎摿堎揑側婍姱傪慡偰徚壔偟丄嵶朎傪儕僙僢僩偡傞偙偲丄偦偺惂屼偼mTOR偱峴傢傟偰偄傞偙偲偑夝偭偰偄傑偡乮2018擭Review)丅 |
偝偰丒丒丒忋婰偺乽堓忋旂壔惗乿乽挵忋旂壔惗乿偱採彞偝傟偰偄傞乽Surface敪娻乿乽Bottom敪娻乿偺擇偮偺儌僨儖偼丄iPS嵶朎乮嵞惗岺妛乯偲嫟捠揰偑懡偄偙偲偑夝傝傑偡丅
椺偊偽乽怱嬝峓嵡屻偵怱嬝嵶朎傪嵞惗偝偣傞乿偲偄偆愴棯偼丄埲壓偺擇捠傝偁傝傑偡丅堦偮偼乽iPS嵶朎壔乿傪宱傞曽朄偱偡丅
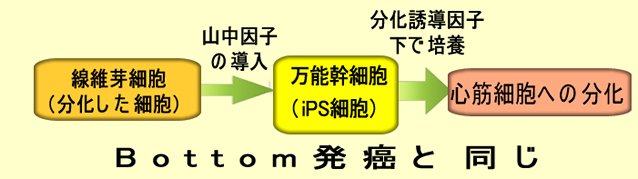
偦偟偰丄傕偆堦偮偼暘壔偟偨嵶朎傪丄捈愙丄懠偺嵶朎偵乽暘壔丒揮姺乿偝偣傞曽朄偱偡丅
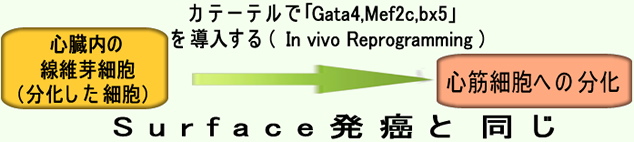
偄偢傟傕儅僂僗偱偼惉岟偟偰偍傝椪彴墳梡傕嬤偄尋媶偱偡偑丄偙偺擇偮偺尰徾偼乽壔惗偱採彞偝傟偰偄傞擇偮偺儌僨儖乿偵懳墳偟偰偄傞偲尵偊傑偡丅
| 偙傟傜偺尰徾偼慡偰丄堚揱巕丗DNA偺曄壔傪敽傢偢丄乽堚揱巕偺廋忺乮僄僺僎僲儉乯乿偩偗偱婲偒傑偡丅嬶懱揑偵偼乽揮幨場巕偺惓偺僼傿乕僪僶僢僋乿偲乽僋儘儅僠儞偺曄壔乿偱乽嵶朎偺暘壔乿偑婲偒傑偡丅佀敪惗妛丄姴嵶朎岺妛偺婎慴乮The Cell丂俀侾乣俀俀復偺梫栺乯偙偺傛偆偵僄僺僎僲儉偩偗偱嵶朎偺暘壔忬懺傪寑揑偵曄偊傞憖嶌傪乽嵞僾儘僌儔儉乮Reprogramming乯乿偲屇傃傑偡丅僇僥乕僥儖側偳傪巊偄丄惉懱撪偱捈愙丄嵶朎偺暘壔忬懺傪曄偊傞憖嶌傪乽In vivo Reprogramming 乿偲屇傃傑偡丅 屄懱偺榁壔偼丄備偭偔傝偲恑峴偡傞乽帺慠偺In vivo Reprogramming 乿偲尵偊傑偡丅iPS嵶朎偺嶌惢偼丄媡偺乽庒曉傝偺Reprogramming 乿偲尵偊傑偡丅 |
俀侽侾俉擭偵嶳拞場巕偵傛傞Reprogramming偵傛傝壔惗乮鋁憻偺ADM壔惗乯偑婲偒丄鋁憻娻偺婋尟偑忋偑傞偲偄偆曬崘偑嫗戝偺iPS尋媶強偐傜Nature偵敪昞偝傟傑偟偨丅曬崘偟偨嶳揷攷巑偼乽iPS壔偲娻偺娭學乿傪尋媶偝傟偰偄傞曽偱偡丅
In vivo reprogramming drives Kras-induced cancer development
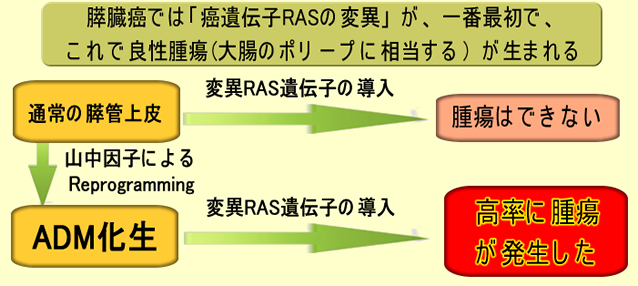
偙偺暋嶨側榖戣偼丄尰嵼丄愱栧壠偱媍榑偵側偭偰偄傑偡乮2022擭Review)丅
| 捛壛帠崁丗枹暘壔娻丒戀帣條娻偺婲尮 徚壔娗偵偼丄嬌傔偰婬偱偡偑乽枹暘壔娻乿偲偄偆乽撪泱梩偺摿幙乿傪姰慡偵幐偭偨娻傗乽拞泱梩丒奜泱梩惉暘傪娷傓婏宍庮揑娻乮戀帣條娻乯乿偑尒傜傟傞偙偲偑偁傝傑偡丅偍偦傜偔偼乽庒曉傝乮Reprogramming乯乿偵傛傝敪惗偟偨偐(2008擭 Nature)丄変乆偺懱撪偵愽傫偱偄傞枩擻姴嵶朎乮MUSE嵶朎乯偺傛偆側嵶朎偑婲尮偐傕偟傟傑偣傫乮昿搙偼嬌傔偰婬偱偁傝MUSE嵶朎偑婋尟偲偄偆堄枴偱偼偁傝傑偣傫乯丅 |
乽庒曉傝偺Reprogramming乿偼幚尡幒偱iPS嵶朎傪嶌惢偡傞帪偩偗偵婲偙傞乽摿庩偱晄帺慠側尰徾乿偱偼側偔丄変乆偺懱撪偱擔忢揑偵婲偒偰偄傞尰徾側偺偐傕偟傟傑偣傫丅
偙偙丄俀乣俁擭丄乽嶳拞場巕傪摫擖偡傞偙偲偱榁壔偟偨儅僂僗傪庒曉傜偣傞偙偲偵惉岟偟偨乿偲偄偆曬崘偑憡師偄偱偄傑偡乮Cell 2017擭丂Nature 2020擭丂Nature 2021擭乯丅屄懱傪庒曉傜偣傞偙偲偼丄嶳拞場巕傪巊偊偽乽幚偼憐憸埲忋偵梕堈偱偁偭偨乿偲偄偆偙偲偱偡丅
椪彴墳梡偵嬤偄In vivo Reprogramming偺寛掕斉偲尵偊傞曬崘偑Nature 2020擭偵偁傝傑偟偨丅傾僗僩儔僛僱僇偺僐儘僫儚僋僠儞偲摨偠曽朄乮堦夁惈敪尰宆僂僀儖僗儀僋僞乕乯偱嶳拞場巕傪摫擖偟 丄榁壔偟偨儅僂僗偺帇椡傪夞暅偝偣傞偙偲偵惉岟偟傑偟偨乮壓恾乯丅
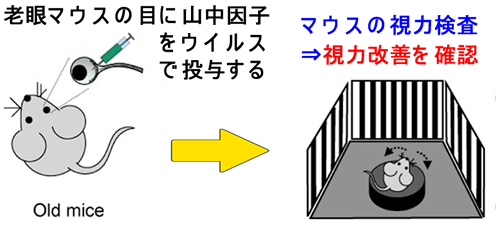
嵞惗岺妛偺恑曕偵偼嬃偔傋偒偱偁傝丄崱屻偼乽庒曉傝丂In vivo Reprogramming 乿偼寖偟偄崙嵺嫞憟偵側傞偱偟傚偆丅堦曽丄偙偺尰徾偵偼乽壔惗乿偲偄偆晄搒崌側暃嶻暔偑敽偆偙偲傕柧傜偐偵側偭偨栿偱偡丅

嶳拞攷巑偑僲乕儀儖徿傪庢傜傟偨帪丄巹偼乽怱憻傗擼偺嵞惗堛椕偑巒傑傞丅偱傕丄帺暘偺愱栧椞堟乮徚壔娗乯偼丄娭學柍偄側丒丒乿偲巚偄傑偟偨丅偟偐偟丄偦傟偼娫堘偄偱丄徚壔娗偺暘栰偱挿偄娫丄廳戝側撲偱偁偭偨乽壔惗乿偲偄偆尰徾偺夝柧偵偮側偑偭偨栿偱偡丅
変乆徚壔婍堛偼丄挿偄娫乽壔惗傪榁壔尰徾乿偲巚偭偰偄傑偟偨丅偟偐偟丄幚偼丄偙傟偼乽変乆偺懱撪偱丄擔乆婲偒偰偄傞庒曉傝偺悘敽尰徾乿偩偭偨栿偱偡丅
