L1僞儞僷僋偼Endocytosis偱丄庢傝崬傑傟僋儔僗嘦採帵佀塼惈柶塽乮拞榓峈懱乯傪桿摫偡傞乮忋昞偺儖乕僩C乯丅捠忢偼嵶朎惈柶塽偼桿摫偟側偄丅偑丄僂僀儖僗傪拞榓偡傞偺偱姶愼杊巭偵側傞丅
偟偐偟庽忬嵶朎偑儚僋僠儞傪庢傝崬傓偲乽岎嵎採帵乿偑婲偙傞偺偱丄堦晹丄嵶朎惈柶塽傕桿摫偝傟傞乮忋昞偺儖乕僩E乯
偟偐偟丒丒丒L1傊偺嵶朎惈柶塽偼丄姶愼嵶朎偺攔彍偵偼栶棫偨側偄
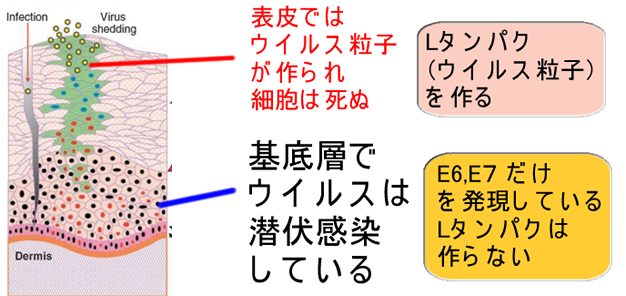
壗屘側傜丒丒丒庮釃壔偟偨嵶朎乮亖帩懕愽暁姶愼乯偼丄偦傕偦傕L1傪敪尰偟側偄偐傜偱偁傞丅
偟偐偟丄椪彴偺曬崘偱偼梊杊儚僋僠儞乮L1儚僋僠儞乯偱傕乽巕媨栩晹Hige Grade CIN偵懳偟偰帯椕岠壥偑偁傞丅乿偲偄偆曬崘偑偁傞丅偙傟偼乮侾乯僂僀儖僗傪峈懱偱拞榓偡傞偺偱嵞姶愼傪杊偖偐傜乮俀乯帩懕愽暁姶愼偱傕彮検偺L侾傪敪尰偟偰偍傝丄岎嵎採帵偱惗傑傟偨CTL偑丄偙傟傪峌寕偟偰偄傞丄偲偄偆擇偮偺壜擻惈偑偁傞丅
偟偐偟丄杮奿揑側帯椕梡儚僋僠儞亖庮釃壔偟偨嵶朎乮亖帩懕愽暁姶愼乯傪嶦偡CTL嵶朎傗僉儔乕嵶朎傪廫暘偵桿摫偡傞偵偼乽E6,E7傪忋昞偺儖乕僩A偐儖乕僩E偱搳梌偡傞乿昁梫偑偁傞丅
E6,E7傪忋昞偺儖乕僩A偱搳梌偡傞帋傒丅
E6,E7傪嵶朎偑撪晹偱揮幨丒東栿偡傞乮儖乕僩A乯昁梫偑桳傞丅扐偟庽忬嵶朎撪偱敪尰偝偣側偗傟偽側傜側偄丅堦斒嵶朎偑奜棃峈尨傪敪尰偟僋儔僗侾採帵偟偰傕僫僀乕僽CD8T嵶朎傪姶嶌偡傞偙偲偼偱偒側偄丅偙傟偼埲慜偺榑憟偩偭偨偑寛拝偑晅偄偰偄傞乮暥專乯丅僫僀乕僽CD8T嵶朎傪姶嶌偱偒傞偺偼庽忬嵶朎偺傒偱偁傞丅
嵶嬠儀僋僞乕乮嵶朎撪怤擖嬠乯丄僂僀儖僗儀僋僞乕丄DNA儚僋僠儞丄RNA儚僋僠儞側偳偑尋媶拞乮暥專乯丅嬃偔傋偒偙偲偵庛撆壔偟偨儕僗僥儕傾嬠乮惗嬠偱偁傞乯傪儀僋僞乕偵巊偆帋傒偑丄尰嵼丄僀儞僪偱恑峴拞乮暥專乯偩偑愭恑崙偱偼愨懳偵擣壜偝傟側偄偩傠偆丅E6,E7傪帩偭偨惗嬠亖恖偑憂憿偟偨乽敪娻惈嵶嬠乿偱偁傞丅SARS-Cov-2偺儚僋僠儞偱偼乽傾僨僲僂僀儖僗儀僋僞乕丄DNA儚僋僠儞丄RNA儚僋僠儞偼奐敪偑抁帪娫偱嵪傓偺偱丄捈偖偵巗応偵弌傞偑丄挿婜揑偵偼岠壥偑掅偄乮嬞媫旔擄揑儚僋僠儞乯乿偙偲偑徹柧偝傟偨偺偱丄偙偺傛偆側怴悽戙儚僋僠儞偑HPV偵墳梡偝傟傞偙偲偼柍偄偲巚傢傟傞丅
E6,E7傪忋昞偺儖乕僩E偱搳梌偡傞帋傒
儖乕僩A偺曽朄傕丄寢嬊偼庽忬嵶朎撪偱敪尰偟側偗傟偽堄枴偑柍偄(忈暻偑崅偄乯偺偩偐傜丄偦傟側傜僞儞僷僋峈尨傪搳梌偟偰庽忬嵶朎偵婷怘偝偣偰岎嵎採帵偝偣偨曽偑崌棟揑偱偁傞丅摉偨傝慜偺榖偱偁傝丄偙偺屆揟揑儖乕僩偑墹摴偲巚傢傟傞丅埲壓偺曽朄偑尋媶拞乮暥專乯丅
乮侾乯嵶朎惈柶塽傪桿摫偡傞傾僕儏僶儞僪偲嫟偵僞儞僷僋丄傑偨偼嫄戝儁僾僠僪傪搳梌偡傞
庽忬嵶朎偑偨偩婷怘偟偨偩偗偱偼岎嵎採帵偑婲偒偢儖乕僩C偟偐婲偒側偄丅偦偙偱岎嵎採帵傪桿婲偡傞傾僕儏僶儞僪偑昁梫偵側傞丅椪彴偱偺桳岠惈偑2009擭偺NEJM偵曬崘偝傟偰偍傝乽帯椕梡HPV儚僋僠儞乿偼婛偵幚梡抜奒偱偁傞丅丅嵶朎惈柶塽桿婲傾僕儏僶儞僪偺尋媶偼艐邅A恑曕偑挊偟偄丅嵟傕桳椡帇偝傟偰偄傞偺偼C-GAMP偱丄摦暔幚尡偱偼乽僀儞僼儖僄儞僓偺慡偰偺宯摑偵桳岠側儐僯僶乕僒儖丒儚僋僠儞乿偑姰惉偟偰偄傞乮暥專乯丅偍偦傜偔丄C-GAMP+E6,E7偑杮柦偲巚傢傟傞丅
乮俀乯MHC僋儔僗嘥寢崌惈偺偁傞儁僾僠僪傪搳梌偡傞
傾僕儏僶儞僪柍偟偱傕岠棪椙偔岎嵎採帵偑婲偙傞丅扐偟丄屄乆偺MHC偵墳偠偰儁僾僠僪傪曄偊傞昁梫偑偁傝崅僐僗僩偵側傞丅
乮俁乯庽忬嵶朎傪攟梴偟偰岎嵎採帵偡傞傛偆偵偟偰偐傜堏怉偡傞丅傑偨偼Adoptive T-cell therapy
崅僐僗僩偱偁傝堦斒壔偼偟側偄偩傠偆偑丄嵟傕岠棪偑崅偄偺偱堦偮偺僆僾僔儑儞偵偼側傞偩傠偆丅
乮係乯岠棪椙偔CD俉T嵶朎乮CTL.僉儔乕乯傪桿摫偟偰傕丄娻偑柶塽摝旔傪偟偰偄傟偽岠棪偼棊偪傞丅僠僃僢僋億僀儞僩慾奞嵻偺暪梡偑廳梫偲偄偆堄尒傕偁傞乮暥專乯丅
彯丄HPV傪攟梴惗嶻偡傞嵶朎宯偼柍偄偨傔丄晄妶壔儚僋僠儞傗庛撆惗儚僋僠儞偺検嶻偼偱偒側偄丅偦偺偨傔丄偦偺傛偆側儚僋僠儞偺尋媶偼柍偄偑丄HPV偺晄妶壔儚僋僠儞偺桳岠惈偼幚尡揑偵妋擣偝傟偰偄傞乮暥專乯丅
