MINEN
��������SMT�ł���A�Ƃ�����
�i�P�j�uNET G2 �ƑB�������݂�������MiNEN�� �P ���v���
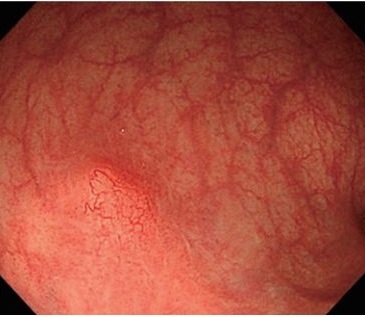
SMT�Ɍ����鑁��MINEN
�i�Q�j
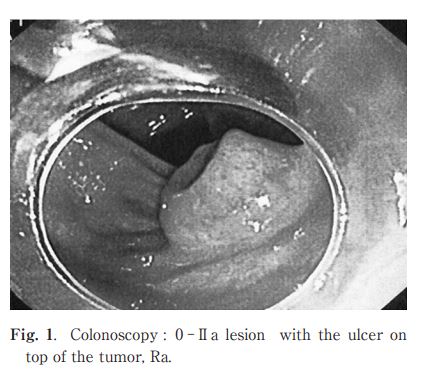
�����̕�������MiNEN��SMT�l�Ɍ�����
NETG1�ƋL�ڂ���Ă���
�i�R�jESD��ɏ�����NETG1�ƑB���̕����a�ςƐf�f���������S������ᇂ�1��
�Ǘ��67�Βj���D�咰�����������Œ�����5�`6mm�̔S������ᇂ�F�߁C1�N��̍Č�����9�`10mm�ɑ���X�����������D�_�o�������ᇁineuroendocrine
tumor�GNET�j�̋^���ŁC�������I�S�����w�����p�iendoscopic submucosal dissection�GESD�j���{�s���CNETG1�ƍ������^�B���̕����a�ςƂ������ɂ܂�Ȏ�ᇂ̐f�f�Ɏ�����
�i�S�j�o�ߊώ@���̂Q�O�~���̒���SMT�i�J���`�m�C�h�j�̒����ɑB��������������
���{������a�w��ҏW�ɂ��I�t�B�V�����ȃK�C�h���C��

�������A�悭�ǂނƁE�E�E�E����Ȃ��Ƃ́AWHO�����ɂ́A�ǂ��ɂ������Ă��Ȃ��i�����j
�uNET��MEN,DAX,ATRX�ُ킪������v�uNEC��P53��RB�ُ�v������u�S���̕ʕ��v
�uMINEN�͑B����NEC�Ɏ��Ă���ANET�Ƃ͕ʕ��v�ł����ᇐi�����낤�Ƃ����b
Shia�̘_���ɂ��A�B���MINEN�̘b�́A�S���L�ڂ��Ȃ��B�����A���L��MESIER�̘_���ƊԈႦ���̂��낤
MESIER�̂Q�O�P�V�N�̉���
Such event can occur at various stages, including early stages such as
adenoma, since cases of MiNEN combining PDNEC and adenoma, without adenocarcinoma,
have been reported�Ƃ��Ĉȉ��̓�̕������Љ��Ă��邪�A�uPDNEC and adenoma�v�̗���u�ɂ߂ċH�v�ƈ�ʓI�Ƃ͌����Ȃ�
�U�U�@Li Y, Yau A, Schaeffer D, Magliocco A, Gui X, Urbanski S, et al: Colorectal
glandular-neuroendocrine mixed tumor: pathologic spectrum and clinical
implications. Am J Surg Pathol 2011;35:413-425
�E���ɑ����B�|���|�C�h�^�������B�B��ˑB����NEC�Ƃ����������咣
�V�P�@Vortmeyer AO, Lubensky IA, Merino MJ, Wang CY, Pham T, Furth EE, et al:
Concordance of genetic alterations in poorly differentiated colorectal
neuroendocrine carcinomas and associated adenocarcinomas. J Natl Cancer
Inst 1997;89:1448-1453.PDNC and associated adenocarcinoma appear to be derived from the same cell
of origin, which is most likely either a pluripotent epithelial stem cell or an adenocarcinoma precursor cell.
|
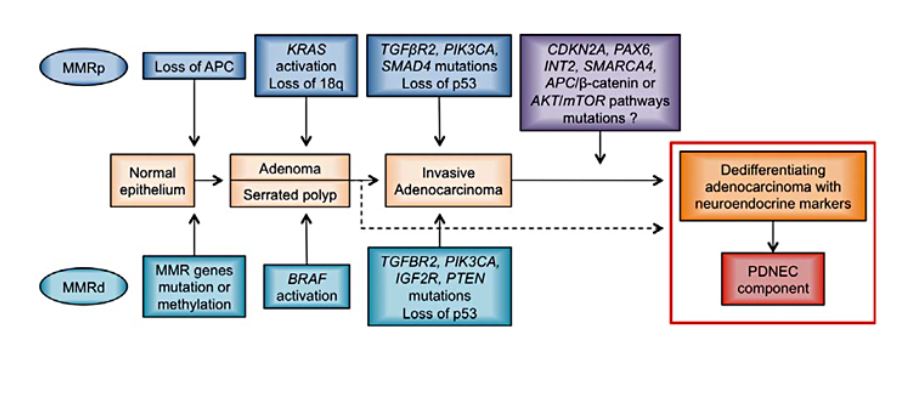
MINEN��PDNEC������Invasive Adenocarcinoma�Ɣ�r���āA�ȉ�����`�q�ψق��lj�����Ă���Ƃ��������������E�E�E�E�ECDKN2A�ȊO�͍�����������
CDKN2A, PAX6�i�N���}�`���C���j, SMARCA4�i�N���}�`���C���j, or INT2 genes,
those encoding for proteins of the APC/��-catenin pathway, or those
involved in the AKT/mTOR pathway.
���d�v���kow �frade MiNEN�iPDNEC�ł͂Ȃ���G1,G2�̂悤�ȕ����^�j�ł͈�`�q�ω��͑B��^�ł͖����āA�ʏ�̃J���`�m�C�h�Ɠ����p�^�[���������B���̌��ۂ���́u���ʋN���v�̕�������
well-differentiated NET components of MiNEN do not harbour similar genetic alterations described in the adenoma/adenocarcinoma counterpart, such as LOH of APC, KRAS, and TP53, but display specific alterations that are usually found in NET (but not PDNEC), such as LOH of VHL
| |
|
CDK2NA |
APC |
|
|
| �X�� |
�B�� |
28% |
2% |
|
|
| PDMEC |
27% |
3% |
|
|
| �咰 |
�B�� |
9% |
50% |
|
|
| PDNEC |
6% |
47% |
|
|
MINEN�̈�`�q�ω��́u��������̑B���Ɏ���v�o�T
�X�ɁuBesides, radiotherapy and chemotherapy might favour genomic instability
and transdifferentiation towards the PDNEC component, based on observations
that the number of neuroendocrine markers-positive cells increased following
neo-adjuvant treatments [18,65]. This strongly suggests that the PDNEC component develops during a classic
adenoma-adenocarcinoma sequence. �v�ƌ������S���Ӗ��s��
MANET�̘_��
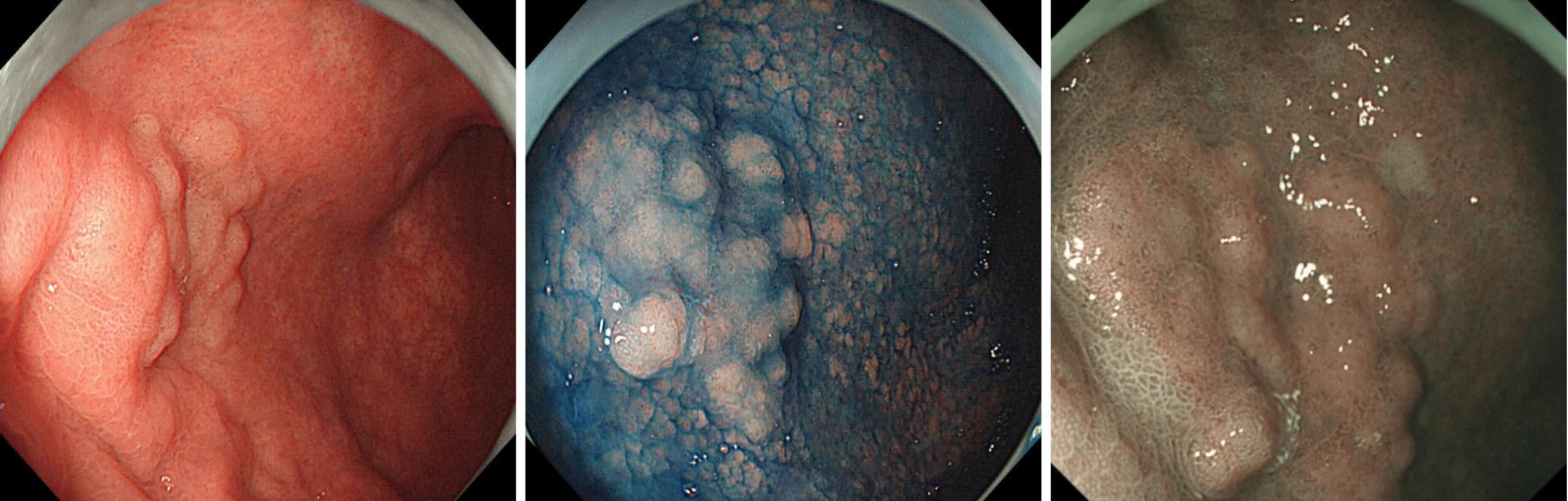
�݂�MANET(2020�N�̕j
Neuroendocrine component is generally located within the deep central portion
of the polyp, whereas the adenomatous component occupies most of the periphery
Endoscopic macroscopic findings included sessile polyps in 5 cases, 0-IIa type polyp
2020�N�̍ŐV�������[
MEEN Mixed epithelial endocrine neoplasms of the colon and rectum
enteroendocrine cells are derived from common precursor gastrointestinal stem cells within the intestinal crypts and do not originate from the neural crest cells
non-neuroendocrine elements in MiNENs are always epithelial (glandular, squamous, mucinous and/or sarcomatoid) and do not include non-epithelial components such as lymphomas[3-9] or mesenchymal components such as smooth muscle tumors
mixed adenoneuroendocrine carcinoma of the pancreas suggests NEC as the precursor giving rise to the adenocarcinoma component, with both of them diverging from a single cancer stem cell
MANEC is a microsatellite stable tumor with strong positivity to CD44 and no expression of maspin suggesting an origin from a CD44-positive stem like precursor cell
In depth mutational analyses by Woischke et al[56] supports the concept of early separation of epithelial and neuroendocrine components during malignant transformation followed by subsequent independent mutational evolution
PDNEC of various origins showed cyclin-dependent kinase Inhibitor 2A/B and APC mutations.
The pathway leading to MSI high NEC/MANECs is the widespread methylation induced silencing of the MLH1 gene as seen in sporadic colorectal carcinomas.
The lack of mutations in ATRX, DAXX, MEN1, and TSC2 also supports a distinctive molecular evolution for the NEC component in comparison to NET tumors
intermediate to high grade colorectal MiNENs exhibit a genetic/molecular profile of identical copy number aberrations, similar to pure colorectal adenocarcinomas though they lack structural chromosomal alterations seen in pure colorectal NEC
Approximately, 5% of colorectal MiNEN are low grade mixed tumors, presenting as polyps < 3 cm in diameter and being composed of tubulovillous or villous adenoma with G1-G2 NET
no alterations are seen of KRAS, BRAF and Pik3CA genes in either tumor component of colonic MANETS.
Another area of continued debate is the WHO discriminatory criterion cut
off 30% rule for each component for inclusion as a mixed tumor. . We strongly recommend
that there should be continued reporting of any second component especially
with poorly differentiated histology or evidence of invasion, regardless
of its percentage volume.
The reasons underlying the presence of only one component in the most distant metastases need to be explored
limited biopsy material as in upto one third of the cases only one of the tumor components is identified
���͏�����NEC�͑��݂��Ȃ��A�Ɨ\�z����Ă���
It is postulated that most pure endocrine cell carcinomas of colon and rectum if examined thoroughly will be associated with a carcinomatous element
somatostatin receptors scintigraphy for the diagnosis and follow-up of MANECs
�i�s�����B�������������ڍׂɒ��ׂ�ƁA�����Ɂu�قȂ镪���������̐����v��������A�����ł͒E�������N���Ă���Ǝv����B���������Ӗ��ł͂R�O�����[�������u�S�Ă̑咰����MiNEN�ł���v�Ƃ����b�ɂȂ�B���ۂɁu�咰���̂R�O����MiNEN�ł���v�Ƃ����ӌ�������
�u�B���˓�������֒E�����v�Ɓu��������ˑB���֒E�����v�ł́A�O�҂̕������|�I�ɕp�x�������̂�����A�i�s����MiNEN�̑����́u�B���˓�������֒E�����v�Ǝv����B����Łi�P�j��������̈�`�q�ُ��NET�����B���ɋ߂��i�Q�j��������̈�`�q�ُ�͑B���̈�`�q�ُ�v���X�A���t�@�i�ł��d�v�Ȃ̂�CDKN2A�j�i�R�j�`�ԓI��Bor�T�`�U�A�ł��邱�Ƃ������ł���
�O���B���ɂ�NeuroEndocrine Cell-Differentiation�Ƃ������ۂ��ǂ��N����炵��
����A�i�P�j������MiNEN���S������ᇗl�ł���i�Q�j��������͈ȑO��NETG3�Ƃ��ĔF������Ă���S������ᇂƔF������Ă������ł͂Ȃ����H�i�R�jMANET�ł͕\�w��B��A�[����NET���z�u����Ă���i�S�jGCC�iGoblet
Cell Cartinoid�j�Ƃ���amphicrine�@tumor���A������
�E�E�E�E�E�E�E�Ƃ������ۂ���́u�������\�������זE�ɋ߂��זE����ᇉ������v�Ƃ������f�����x�������
��s�����̇Tsp�^�@MinEN�̕�
High grade evolution of a MANET���f��
primary high grade NEC rarely occurs in patients with FAP in contrast to neuroendocrine hyperplasia and well differentiated NET supporting the theory that the evolution of NEC is distinct from NET in these mixed tumors
����i�n�Ӌ����j���Q�O�P�V�N�ɏo�����l�`�m�d�b�̘_��
MiNEN�ƒʏ�̑咰����CF�ł́A��ʂł��Ȃ��BNET�̂悤��SMT�̌`�Ԃ��Ƃ�Ȃ��BMANEC�̂قƂ�ǂ�Borrman�T���U�ł���
Colorectal mixed adenoneuroendocrine carcinomas and neuroendocrine carcinomas are genetically closely related to colorectal adenocarcinomas �Q�O�P�V�N�_��
Our data indicate that colorectal mixed adenoneuroendocrine carcinomas
and neuroendocrine carcinomas are genetically closely related to colorectal
adenocarcinomas, suggesting that the cells giving rise to these tumors
primarily have an intestinal coinag
Point mutations in neuroendocrine neoplasm-related genes like RB1 or RET
were not detected
RET���������ᇁA�b��B���ŗz���BMEN�̂悤�Ȃ���
RET��RB1���J���`�m�C�h�iNET�j�̃}�[�J�[�ɂȂ�B������NEC�ł́A�����ُ̈�͖���
Amphicrine carcinoma �Ƃ����T�O
Previous studies had demonstrated the excellent performance of the 90-gene expression signature for identification of tumor origin [10, 35]. After hierarchical clustering of the gene expression magnitudes, the
pan-cancer panel reflected the similarity between the mRNA expression profile
in amphicrine carcinoma and traditional adenocarcinoma, with no relationship
between the amphicrine carcinoma and NET profiles.
GCC�ɂ���
������Amphicrine tumors���u�t�זE�J���`�m�C�h�iGCC�j�ƔS�t���̗��������v�̕@�Q�O�P�S�N
GCC�͎�ɒ����Ɍ�����B�O����Ɠ�����̗����̐��������B�u������MINEN�v�B�������\���זE���甭������Ƃ����������uunitary intestinal stem cell theory�v�ƌĂԁiUnitarian Theory of the origin of the four epithelial cell types.�Ɠ����l���j�BGCC�͔S�t���AMINEN,��ӍזE���Ɛ[���W������͂��ł���B
�Q�O�P�W�N�@GCC�͗\�オ�����B�܂��S�t�Y������}�����������N�����Ղ�
2021�@appendiceal neuroendocrine tumors (ANETs) low-grade appendiceal mucinous
neoplasm (LAMN) �̍���

